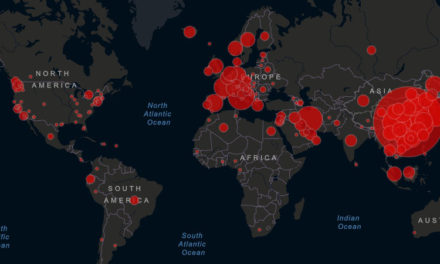
GUÍA PARA ENTENDER LOS MUTANTES Y LAS VARIANTES DEL SARS-COV-2
Texto: Ignacio López-Goñi. Catedrático Universidad de Navarra
Imágenes: Cortesía Google
Los virus mutan constantemente, viven mutando. Una población de virus es una nube de mutantes, con pequeñas diferencias genéticas. Se han detectado ya varios miles de tipos de SARS-CoV-2. La mayoría no tiene efecto ni interés alguno.
¿El coronavirus muta poco o mucho? Mucho, pero depende de con quién se le compare.
El virus de la gripe y el VIH probablemente sean los campeones de la variabilidad. El primero tiene un genoma de ARN, y la enzima que lo copia es muy torpe e introduce muchos errores al hacerlo. Estos no se reparan con la misma eficacia que en los virus con genoma de ADN (cuya polimerasa es una enzima más precisa).
Los coronavirus mutan poco. Pero mutan, claro.
Además, el virus de la gripe está formado por entre 7 y 8 fragmentos de ARN, que pueden mezclarse o recombinar entre sí con frecuencia cuando coinciden varios virus en una misma célula. Este patógeno es propio de las aves, pero frecuenta otros muchos animales, que actúan como almacén y fuente de nuevas cepas. Todo esto hace que sea uno de los virus con mayor frecuencia de mutación y recombinación (en palabras técnicas, deriva y desviación antigénica).
Por su parte, el VIH también tiene genoma ARN, pero su replicación depende de una enzima viral, la retrotranscriptasa o transcriptasa inversa, que copia el genoma ARN en forma de ADN. Esta es todavía más torpe, y mete más mutaciones. Además, el VIH tiene dos copias idénticas de ARN, lo que también aumenta su capacidad de recombinación.
Comparado con estos dos campeones, los coronavirus mutan poco. Pero mutan, claro. También son virus de ARN y también tienen una polimerasa torpe, pero su genoma es solo un fragmento de ARN muy grande de unos 30 000 pares de bases.
Como no pueden permitirse muchos errores, tienen una enzima cuya función es reparar los que comete la polimerasa al hacer copias del genoma. Esta menor frecuencia de mutación y recombinación nos permite hablar de “variantes genéticas”.
Algunos han calculado que esa frecuencia de mutación es de dos mutaciones al mes, lo que supone que las variantes que ahora circulan pueden haber acumulado unas 26 mutaciones respecto a la secuencia original del primer aislamiento de Wuhan. Hasta ahora se han descrito miles, la mayoría sin ningún efecto en el virus.
Cuando hablamos de mutaciones nos referimos al genoma de ARN o ADN. Lo que muta son los ácidos nucleicos, no las proteínas, aunque esto se manifieste en forma de cambio en éstas.
La famosa mutación en la proteína S del coronavirus llamada N501Y.
Tomemos la famosa mutación en la proteína S del coronavirus llamada N501Y. ¿Qué significa? Los números hacen referencia al número del aminoácido en la proteína, y las siglas al tipo de aminoácido. En este caso concreto, ha habido una mutación en el gen que codifica (que lleva la información) para la proteína S, de forma que hay un cambio en el aminoácido 501 de la proteína, y se sustituye el aminoácido Asparragina (N) por la Tirosina (Y): N501Y.
A la caza de mutaciones y variantes
Desde febrero del año pasado se secuencian genomas de SARS-CoV-2. Esto ha permitido seguir la evolución a tiempo real del virus y la aparición de nuevos mutantes. Hay ya más de 260 000 secuencias disponibles en las bases de datos. Estas provienen de otros tantos aislamientos obtenidos de muestras humanas desde febrero del año pasado hasta el momento actual. Aunque los cambios de nucleótidos son la primera fuente de variación genética del SARS-CoV-2, también se han detectado inserciones, deleciones e incluso recombinaciones.
Los cambios de nucleótidos son la primera fuente de variación genética del SARS-CoV-2
Estos análisis de las mutaciones permiten hacer filogenias (relaciones de parentesco) que pueden emplearse para:
- Hacer estimaciones temporales (cuándo surgen nuevas variantes)
- Caracterizar cómo se extiende geográficamente el virus.
- Reconstruir la dinámica epidemiológica dentro de una región.
- Analizar cómo se adapta a lo largo del tiempo.
El análisis de las secuencias del SARS-CoV-2 no tiene precedentes. En la base de datos GISAID (Global Initiative on Sharing Avian Influenza Data), hay más de 700 000 datos de secuencias compartidas. Es la primera vez que se está siguiendo a tiempo real la evolución de un virus pandémico.
Lo que interesa es estudiar qué mutaciones van apareciendo en el genoma de SARS-CoV-2 a lo largo del tiempo y qué efecto pueden tener. Las variantes acumulan varias de ellas. El término cepa se reserva a variantes con cambios importantes (antigenicidad, transmisibilidad, virulencia) y de momento no se utiliza con el coronavirus.
Variantes de interés y preocupación
De todas las mutaciones las que más preocupan son las que afectan al gen que codifica para la proteína S. Esta interacciona con el receptor celular ACE2 (la puerta de entrada a la célula), lo que podría afectar a su transmisibilidad.
Además, al ser la proteína más expuesta es también la más antigénica, sobre la que actúan los anticuerpos. La mayoría de las vacunas la utilizan como estrategia para activar el sistema inmune. Interesa, por tanto, controlar el número de mutaciones que se van acumulando y el gen concreto al que afectan.
Las mutaciones más relevantes en estos momentos son N501Y y E484K, en el gen de la proteína S. Están presentes en varias de las variantes genéticas y el hecho de que estén apareciendo de manera independiente en varios grupos o linajes sugiere que confieren una ventaja adaptativa al virus.
Sistema inmunológico atacando un coronavirus.
Las mutaciones y, por tanto, las nuevas variantes irán apareciendo de forma espontánea en cualquier lugar y en cualquier momento. Nos vamos a encontrar muchas. Así se van construyendo los árboles filogenéticos que muestran cómo evoluciona el genoma del virus y se diferencia en distintos grupos o linajes.
Al estudiar las variantes distinguimos lo que se denomina, Variante de Interés (VOI), Variante Preocupante o de Importancia (VOC).
Una variante de interés tiene mutaciones que conducen a cambios de aminoácidos asociados con sospechas de implicaciones fenotípicas. Además, ha sido identificada como causante de transmisión comunitaria o detectada en varios países.
Una variante de interés pasaría a ser preocupante si se demuestra que, además, está asociada con un aumento de la transmisibilidad o virulencia, un cambio en la presentación clínica de la enfermedad o una disminución de la eficacia de las medidas sociales y de salud pública, vacunas y tratamientos incluidos.
En los últimos meses se han ido encontrado nuevas variantes que preocupan porque son más infectivas, es decir, que una persona necesita inhalar menos virus para infectarse. Otras son más transmisibles, que significa que aumentan la cantidad de virus que desprende una persona. Otras parecen tener más facilidad para evadir los anticuerpos del sistema inmune.
La Variante Británica.
Las variantes que podríamos clasificar de preocupantes en este momento son la británica (B.1.1.7), la brasileña (P.1), y la sudafricana (B.1.351).
Las variantes surgen en cualquier momento y en cualquier lugar. Detectarlas depende de nuestra capacidad de buscarlas y encontrarlas por secuenciación. Como era de esperar, desde hace unas semanas, se han ido describiendo otras variantes de interés por distintas partes del planeta.
Así, se habla de la variante B.1.429/427 de California, que parece que es algo más transmisible pero no hay datos, de momento, que la asocien con una mayor virulencia y escape inmune. La B.1.526 de Nueva York, también quizá más transmisible y que preocupa porque ha aparecido en un área donde había un alto nivel de inmunidad (esa ciudad fue uno de los focos de la pandemia en EE. UU. la primavera pasada). Todavía hay más, como la P.2 (brasileña de Río de Janeiro), B.1.525 (o nigeriana), VOC 202102/02 (muy similar a la británica), C.16 (de Portugal) y A.23.1 (detectada en Reino Unido).
¿Qué se vigila en una nueva variante?
- El número de mutaciones (si tiene muchas) y dónde las tiene.
- Si aumenta rápidamente su frecuencia entre la población.
- Si presenta las mismas mutaciones que otras variantes, lo que puede sugerir, como hemos comentado, un fenómeno de evolución convergente y ventaja adaptativa.
- Si se extiende en áreas donde ya hay un alto nivel de inmunidad contra el SARS-CoV-2 (porque haya habido un alto nivel de infección natural o alta cobertura vacunal).
Solo la vigilancia y la investigación demostrarán si estas nuevas variantes pasan a la siguiente categoría de variantes de preocupación. Hacen falta evidencias científicas que demuestren qué efecto pueden tener estas nuevas variantes en la infectividad, transmisibilidad y evasión del sistema inmune.
Un término que han acuñado en inglés es el de “scariants”, que podríamos traducir como “variante terrorífica”, y hace referencia a esas variantes de las que en realidad todavía tenemos muy pocos datos experimentales y sabemos muy poco, pero que son noticia en la prensa y alarman sugiriendo que van a suponer volver al inicio de la pandemia.
Vacunación contra variante del C19. Imagen de Angelo Esslinger-Pixabay.
¿Podría ocurrir? No lo sabemos, pero normalmente la transmisibilidad y la letalidad no suelen evolucionar a la vez. Recordemos que el virus, independientemente del tipo de variante, ya es muy contagioso y peligroso y las medidas que tenemos que tomar contra las nuevas variantes son las mismas que contra el virus nativo: evitar contagios y vacunar.
El efecto que puedan tener las variantes en el desarrollo de la pandemia todavía es incierto, estamos en un momento delicado de incertidumbre. Es pronto todavía para saber cómo podrían influir en la efectividad de las vacunas, aunque haya datos sobre que los anticuerpos de personas vacunadas reaccionen algo menos con algunas de estas variantes.
Hay que tener en cuenta que las vacunas no solo inducen anticuerpos neutralizantes, sino que además, activan la inmunidad celular, que en el caso de los coronavirus, juega un papel más importante que los anticuerpos. Una prepublicación pendiente de revisión por pares, muestra que la respuesta inmune celular (dependiente de linfocitos T CD4 y CD8), de personas que han pasado la covid-19 o han sido vacunadas con las vacunas de ARNm no se ve afectada por las nuevas variantes del SARS-CoV-2.
De momento, dediquemos tiempo a secuenciar e investigar y a evitar que se extienda el virus. Cuanta más gente infectada haya, más virus habrá en el ambiente y más posibilidad de que surjan nuevas variantes. Por eso hay que vacunar, vacunar y vacunar.
Articulista
Prof. Dr. Ignacio López-Goñi. Catedrático de Microbiología de la Universidad de Navarra. Doctor en Biología por la Universidad de Navarra (1989)
Durante varios años fue investigador del Instituto Nacional de Investigaciones Agrarias (INIA) en los Departamentos de Biología Molecular y Celular de la Universidad de Berkeley (California, EE.UU.) y de Microbiología Molecular de la Universidad de Columbia (Missouri, EE.UU.) Desde agosto de 1992 se incorporó como Profesor en el Departamento de Microbiología y Parasitología de la Universidad de Navarra, donde ha impartido Microbiología general y Virología en los grados de Biología, Bioquímica y Farmacia. Durante 2005-2014 fue Decano de la Facultad de Ciencias de la Universidad de Navarra.
Su investigación se ha centrado en el estudio de los mecanismos moleculares y genéticos que controlan la virulencia de las bacterias patógenas, el desarrollo de nuevas vacunas contra la brucelosis y de nuevos métodos de diagnóstico de enfermedades infecciosas. Ha participado como Investigador en varios proyectos nacionales y europeos y ha sido director de siete tesis doctorales (una de ellas Premio SYVA 2010 a la mejor tesis en Sanidad Animal). Fue Presidente de la Sociedad Internacional de Brucelosis, autor de varias publicaciones especializadas, editor de dos libros sobre microbiología molecular y genómica de la bacteria Brucella. Es Vicepresidente del grupo de Docencia y Difusión de la Microbiología de la Sociedad Española de Microbiología y miembro de la American Society for Microbiology.
Compagina su labor docente e investigadora con una intensa actividad de divulgación científica a través de blogs, redes sociales y cursos masivos online (MOOC). Es autor del blog “microBIO” y “El rincón de Pasteur” de la revista Investigación y Ciencia. Ha publicado varios libros divulgativos: “¿Funcionan las vacunas?”, “Virus y pandemias”, «Microbiota: los microbios de tu organismo». En 2016 recibió el premio Tesla de divulgación científica, y en 2017 el premio ASEBIO 2017 de Comunicación y Divulgación de la Biotecnología, en la Categoría prensa digital y nuevos medios.